Mitomycin C的作用機制及在腫瘤細胞系和動物模型中的多場景應用
Mitomycin C(絲裂霉素C,MMC,AbMole,M5791)是一種從鏈霉菌屬(Streptomyces caespitosus)發(fā)酵產(chǎn)物中分離得到的醌類抗生素。Mitomycin C具有一定的腫瘤抑制活性,它通過抑制細胞增殖和DNA合成發(fā)揮抑制作用。AbMole為全球科研客戶提供高純度、高生物活性的抑制劑、細胞因子、人源單抗、天然產(chǎn)物、熒光染料、多肽、靶點蛋白、化合物庫、抗生素等科研試劑,全球大量文獻專利引用。
一、Mitomycin C(絲裂霉素C)作用機制
Mitomycin C(絲裂霉素C,MMC,AbMole,M5791)在細胞內(nèi)的低氧或還原環(huán)境下,如腫瘤細胞微環(huán)境中,MMC的苯醌環(huán)可被 NADPH-細胞色素P450還原酶或DT-二氫葉酸還原酶還原為氫醌衍生物,隨后氫醌衍生物自發(fā)氧化釋放活性氧(ROS)并生成烷化劑,上述烷化劑能夠與DNA的鳥嘌呤(G)N-2位點發(fā)生烷基化反應。同時,其苯醌環(huán)的另一活性位點可與相鄰 DNA 鏈的鳥嘌呤或胞嘧啶(C)形成共價交聯(lián),最終導致 DNA 雙鏈交聯(lián)(DSC),嚴重阻礙 DNA 的復制和轉(zhuǎn)錄過程,使得細胞無法正常進行遺傳信息的傳遞和表達,從而對細胞的增殖和功能產(chǎn)生抑制作用。
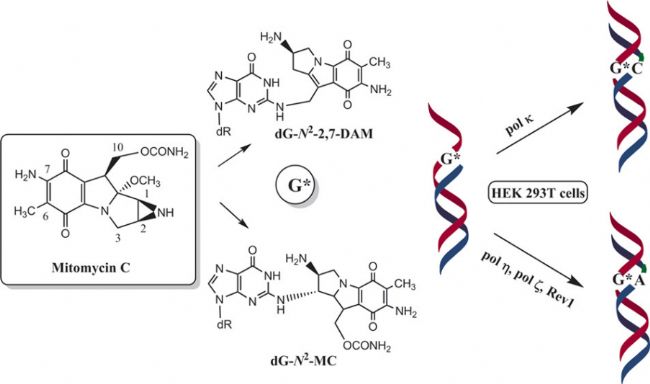
圖 1. Mitomycin C的作用機理[1]
除了 DNA 交聯(lián)作用外,Mitomycin C(絲裂霉素C,MMC,AbMole,M5791)在氧化還原循環(huán)過程中會產(chǎn)生大量ROS,進而攻擊細胞內(nèi)的生物大分子,包括脂質(zhì)、蛋白質(zhì)和核酸等。引發(fā)氧化應激反應,加劇細胞損傷,最終誘導細胞凋亡或壞死。最近的研究發(fā)現(xiàn),Mitomycin C對硫氧還蛋白還原酶(Thioredoxin Reductase, TrxR)具有抑制作用[2]。Mitomycin C對TrxR的抑制可能導致細胞內(nèi)氧化應激水平升高,進而影響細胞的抗氧化防御系統(tǒng)。
二、研究應用
1.Mitomycin C(絲裂霉素C)用于腫瘤研究
在腫瘤細胞系研究中,MMC (絲裂霉素C,Mitomycin C,AbMole,M5791)可用于評估其對腫瘤細胞增殖、遷移和侵襲能力的影響。通過體外實驗,觀察Mitomycin C處理后腫瘤細胞的克隆形成能力、細胞劃痕愈合速度以及穿過 Transwell 小室的能力變化,研究腫瘤細胞的惡性生物學行為,篩選潛在的腫瘤抑制靶點。Mitomycin C可用于抑制膀胱癌、胃癌、頭頸部腫瘤、乳腺癌、胰腺癌、非小細胞肺癌等多種腫瘤細胞系[3]。
2.Mitomycin C用于其它動物模型的研究
Mitomycin C(絲裂霉素C,Mitomycin C,AbMole,M5791)還是一種動物實驗慢性傷口造模劑,經(jīng)Mitomycin C處理組的大鼠后背傷口愈合速度更慢,疤痕組織形成減少,且出現(xiàn)了壞死組織。傷口呈現(xiàn)棕色、干燥、厚實的慢性傷口特征,愈合時間比對照組長[4]。在食管化學損傷模型中,局部應用MMC具有增益效果,尤其是在損傷后立即使用[5]。Mitomycin C還能夠用于聲帶損傷模型的愈合[6]。此外,利用Mitomycin C還可構(gòu)建大鼠肺靜脈閉塞模型,通過給SD大鼠注射2 mg/kg的Mitomycin C,然后觀察肺組織的炎癥細胞浸潤、肺泡壁增厚和肺靜脈閉塞情況。MMC處理的肺組織顯示出肺泡壁增厚、炎癥細胞浸潤和肺靜脈閉塞等變化,證實模型的成功構(gòu)建[7]。2014年,AbMole的兩款抑制劑分別被西班牙國家心血管研究中心和美國哥倫比亞大學用于動物體內(nèi)實驗,相關(guān)科研成果發(fā)表于頂刊 Nature 和 Nature Medicine。
三、范例詳解:
Front Immunol. 2023 May 1;14:1182851.
中山大學第一附屬醫(yī)院的實驗人員在上述論文中探究了DNA依賴的IFN調(diào)節(jié)因子(DAI),在樹突狀細胞(DCs)成熟中的作用,以及抑制DAI對小鼠胰島和皮膚異體移植存活的影響。實驗人員使用重組腺病毒載體(AdV-DAI-RNAi-GFP)轉(zhuǎn)導小鼠骨髓來源的樹突狀細胞(BMDCs),以抑制DAI表達(DC-DAI-RNAi),并評估其在脂多糖(LPS)刺激下的免疫細胞表型和功能。在胰島移植和皮膚移植前,將DC-DAI-RNAi注入受體小鼠,記錄胰島和皮膚異體移植的存活時間,并測量脾臟中T細胞亞群的比例和血清中細胞因子的分泌水平。在文章中,AbMole的Mitomycin C(絲裂霉素C,Mitomycin C,AbMole,M5791)用于處理DCs,以抑制其在混合淋巴細胞反應(MLR)中的增殖能力(Mitomycin C可用于處理抗原呈遞細胞以避免其在反應過程中發(fā)生自主增殖,從而確保反應的特異性和可分析性)。
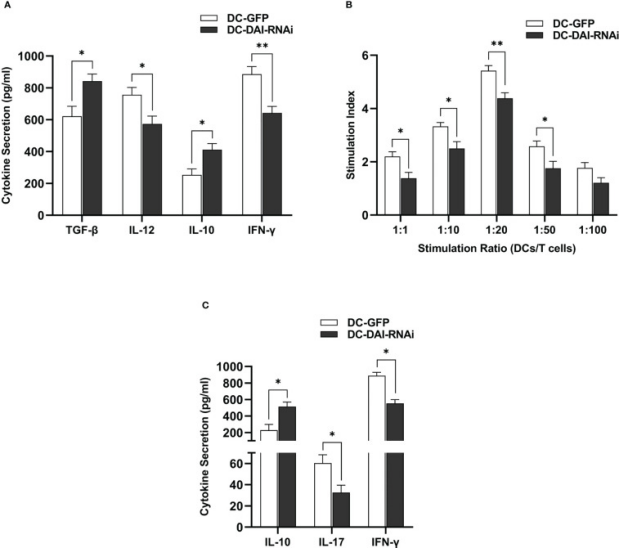
圖 2. DC-DAI-RNAi exhibited the immunosuppressive properties of tolerogenic DCs[8]
參考文獻及鳴謝
[1] A. Bose, C. Surugihalli, P. Pande, E. Champeil, A.K. Basu, Comparative Error-Free and Error-Prone Translesion Synthesis of N(2)-2'-Deoxyguanosine Adducts Formed by Mitomycin C and Its Metabolite, 2,7-Diaminomitosene, in Human Cells, Chem Res Toxicol 29(5) (2016) 933-9.
[2] M.M. Paz, X. Zhang, J. Lu, A. Holmgren, A new mechanism of action for the anticancer drug mitomycin C: mechanism-based inhibition of thioredoxin reductase, Chem Res Toxicol 25(7) (2012) 1502-11.
[3] J.H. Beijnen, H. Lingeman, H.A. Van Munster, W.J. Underberg, Mitomycin antitumour agents: a review of their physico-chemical and analytical properties and stability, J Pharm Biomed Anal 4(3) (1986) 275-95.
[4] A. Ariawan, A. Wicaksana, A. Rifqi Fauzi, R. Seswandhana, Chronic wound mitomycin-c-induced animal models, Journal of thee Medical Sciences (Berkala Ilmu Kedokteran) 50(2) (2018).
[5] T.F. Bustamante, P.L. Lourenção, K.L. Higa, A.P. Silva, E.V. Ortolan, The use of mitomycin C in caustic esophagitis in rats, Acta Cir Bras 28(2) (2013) 136-41.
[6] C.G. Garrett, J. Soto, J. Riddick, C.R. Billante, L. Reinisch, Effect of mitomycin-C on vocal fold healing in a canine model, Ann Otol Rhinol Laryngol 110(1) (2001) 25-30.
[7] Q. Song, P. Chen, S.J. Wu, Y. Chen, Y. Zhang, Differential Expression Profile of microRNAs and Tight Junction in the Lung Tissues of Rat With Mitomycin-C-Induced Pulmonary Veno-Occlusive Disease, Front Cardiovasc Med 9 (2022) 746888.
[8] P. Cheng, Q. Jian, Z. Fu, R. Deng, Y. Ma, Inhibition of DAI refrains dendritic cells from maturation and prolongs murine islet and skin allograft survival, Front Immunol 14 (2023) 1182851.
標簽:
絲裂霉素C
Copyright(C) 1998-2025 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com