抗體偶聯(lián)藥物的核心優(yōu)勢(shì)及未來(lái)對(duì)腫瘤治療的影響
在癌癥治療的漫長(zhǎng)征程中,如何實(shí)現(xiàn) “精準(zhǔn)打擊癌細(xì)胞而不傷及無(wú)辜” 始終是醫(yī)學(xué)界的核心課題。抗體偶聯(lián)藥物(Antibody-Drug Conjugates, ADC)的出現(xiàn),宛如為藥物裝上了 “制導(dǎo)系統(tǒng)”,讓化療藥物從 “地毯式轟炸” 升級(jí)為 “精準(zhǔn)導(dǎo)彈打擊”。這種融合抗體靶向性與細(xì)胞毒藥物殺傷力的創(chuàng)新療法,正以年均 40% 的市場(chǎng)增速改寫(xiě)腫瘤治療格局,成為繼化療、靶向藥、免疫治療后的第四大癌癥治療支柱。
一、ADC 的 “三位一體” 設(shè)計(jì):從概念到現(xiàn)實(shí)的醫(yī)藥工程學(xué)突破
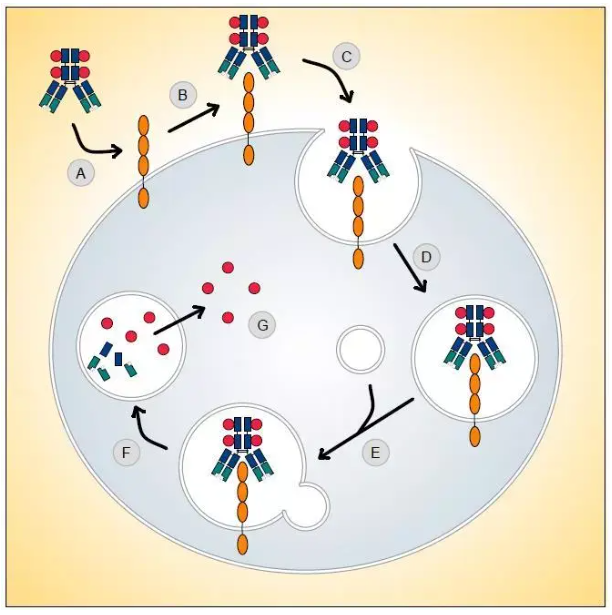
ADC 的精妙之處在于其 “導(dǎo)彈式” 分子架構(gòu),由三大核心組件協(xié)同完成 “精準(zhǔn)制導(dǎo) - 定點(diǎn)爆破 - 安全釋放” 的高效殺傷:
1. 抗體 “制導(dǎo)系統(tǒng)”:靶向癌細(xì)胞的 “生物 GPS”
單克隆抗體(如曲妥珠單抗、帕妥珠單抗)經(jīng)過(guò)基因工程改造,能精準(zhǔn)識(shí)別癌細(xì)胞表面高表達(dá)抗原(如 HER2、Trop-2、Claudin 18.2)。這些抗原如同癌細(xì)胞的 “獨(dú)特門(mén)牌”,引導(dǎo) ADC 富集于腫瘤組織,相比傳統(tǒng)化療藥物的全身擴(kuò)散,可實(shí)現(xiàn) 10-100 倍的腫瘤部位藥物濃度富集。
2. 毒素 “戰(zhàn)斗部”:高效低毒的新一代細(xì)胞殺手
不同于傳統(tǒng)化療藥物(如紫杉醇、阿霉素),ADC 搭載的小分子毒素經(jīng)過(guò)特殊設(shè)計(jì):
連接子如同導(dǎo)彈的 “保險(xiǎn)裝置”,需滿(mǎn)足雙重要求:
二、ADC 的 “降維打擊” 優(yōu)勢(shì):三大核心特性重塑治療邏輯
1. 突破靶向治療耐藥困境
當(dāng)靶向藥因抗原突變(如 EGFR T790M)或信號(hào)通路旁路激活失效時(shí),ADC 可通過(guò) “旁觀者效應(yīng)” 擴(kuò)大殺傷范圍 —— 釋放的毒素能穿透細(xì)胞膜,殺滅鄰近未表達(dá)靶抗原的癌細(xì)胞,尤其適合異質(zhì)性強(qiáng)的實(shí)體瘤(如三陰乳腺癌、非小細(xì)胞肺癌)。
2. 解鎖 “不可成藥” 靶點(diǎn)
針對(duì)傳統(tǒng)靶向藥難以作用的膜蛋白(如糖蛋白、黏附分子),ADC 展現(xiàn)獨(dú)特優(yōu)勢(shì):
ADC 的療效與 “藥物抗體比”(DAR)密切相關(guān),通過(guò)控制每個(gè)抗體連接 2-8 個(gè)毒素分子,在保證靶向性的同時(shí)避免抗體結(jié)構(gòu)破壞。以 HER2 陽(yáng)性乳腺癌為例,曲妥珠單抗 ADC(T-DXd)的 DAR 值達(dá) 8,較傳統(tǒng) T-DM1(DAR=3.5)療效提升 3 倍,且心臟毒性顯著降低。
三、全球市場(chǎng)爆發(fā):從 “小眾創(chuàng)新” 到 “百億賽道”
當(dāng)前全球已上市 16 款 ADC 藥物,2023 年市場(chǎng)規(guī)模達(dá) 138 億美元,預(yù)計(jì) 2030 年將突破 600 億美元,三大驅(qū)動(dòng)力加速行業(yè)變革:
1. 適應(yīng)癥快速擴(kuò)展
從血液瘤(如 CD19 ADC 治療 B 細(xì)胞淋巴瘤)到實(shí)體瘤(如 HER2 ADC 覆蓋胃癌、肺癌、乳腺癌),ADC 適應(yīng)癥已覆蓋 12 大癌種,僅 2023 年就有 5 款新藥獲批,包括首個(gè)雙特異性 ADC(REGN1500/RG7802)。
2. 技術(shù)平臺(tái)迭代升級(jí)
榮昌生物(RC48)、恒瑞醫(yī)藥(SHR-A1811)、科倫博泰(SKB264)等本土企業(yè)引領(lǐng) ADC 研發(fā),全球在研 ADC 中 35% 來(lái)自中國(guó),適應(yīng)癥覆蓋 HER2、Claudin 18.2、c-Met 等熱門(mén)靶點(diǎn),部分產(chǎn)品(如 RC48)已獲 FDA 突破性療法認(rèn)定,開(kāi)啟 “中國(guó)創(chuàng)新藥出海” 新征程。
四、挑戰(zhàn)與未來(lái):從技術(shù)攻堅(jiān)到生態(tài)構(gòu)建
1. 三大核心技術(shù)瓶頸
結(jié)語(yǔ):ADC 開(kāi)啟腫瘤治療 “精準(zhǔn)爆破” 時(shí)代
從 1913 年保羅・埃爾利希提出 “魔法子彈” 概念,到 2023 年 ADC 全球市場(chǎng)突破百億,人類(lèi)用百年時(shí)間將夢(mèng)想轉(zhuǎn)化為現(xiàn)實(shí)。這種融合抗體靶向性、毒素高效性、連接子智能性的創(chuàng)新藥物,不僅改寫(xiě)了 HER2 等經(jīng)典靶點(diǎn)的治療格局,更解鎖了眾多 “不可成藥” 靶點(diǎn)的治療潛力。
杭州斯達(dá)特 (www.starter-bio.com)志在為全球生命科學(xué)行業(yè)提供優(yōu)質(zhì)的抗體、蛋白、試劑盒等產(chǎn)品及研發(fā)服務(wù)。依托多個(gè)開(kāi)發(fā)平臺(tái):重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開(kāi)發(fā)平臺(tái)(E.coli,CHO,HEK293,InsectCells),已正式通過(guò)歐盟98/79/EC認(rèn)證、ISO9001認(rèn)證、ISO13485。
一、ADC 的 “三位一體” 設(shè)計(jì):從概念到現(xiàn)實(shí)的醫(yī)藥工程學(xué)突破
ADC 的精妙之處在于其 “導(dǎo)彈式” 分子架構(gòu),由三大核心組件協(xié)同完成 “精準(zhǔn)制導(dǎo) - 定點(diǎn)爆破 - 安全釋放” 的高效殺傷:
1. 抗體 “制導(dǎo)系統(tǒng)”:靶向癌細(xì)胞的 “生物 GPS”
單克隆抗體(如曲妥珠單抗、帕妥珠單抗)經(jīng)過(guò)基因工程改造,能精準(zhǔn)識(shí)別癌細(xì)胞表面高表達(dá)抗原(如 HER2、Trop-2、Claudin 18.2)。這些抗原如同癌細(xì)胞的 “獨(dú)特門(mén)牌”,引導(dǎo) ADC 富集于腫瘤組織,相比傳統(tǒng)化療藥物的全身擴(kuò)散,可實(shí)現(xiàn) 10-100 倍的腫瘤部位藥物濃度富集。
2. 毒素 “戰(zhàn)斗部”:高效低毒的新一代細(xì)胞殺手
不同于傳統(tǒng)化療藥物(如紫杉醇、阿霉素),ADC 搭載的小分子毒素經(jīng)過(guò)特殊設(shè)計(jì):
- 高殺傷力:?jiǎn)渭谆鶌W瑞他汀(MMAE/MMAF)、喜樹(shù)堿衍生物(SN-38)等毒素的殺傷力較常規(guī)化療藥強(qiáng) 100-1000 倍,僅需 1-2 個(gè)分子進(jìn)入細(xì)胞即可誘導(dǎo)凋亡;
- 低免疫原性:通過(guò)合成化學(xué)修飾降低毒素免疫反應(yīng),避免引發(fā)全身性炎癥。
連接子如同導(dǎo)彈的 “保險(xiǎn)裝置”,需滿(mǎn)足雙重要求:
- 循環(huán)穩(wěn)定性:在血液中保持穩(wěn)定,避免毒素提前釋放損傷正常細(xì)胞(如聚乙烯 glycol 修飾提升水溶性);
- 微環(huán)境響應(yīng):到達(dá)腫瘤后,通過(guò) pH 敏感(腫瘤微環(huán)境 pH 6.5-6.8)、酶解(組織蛋白酶 B)或還原(谷胱甘肽)機(jī)制精準(zhǔn)釋放毒素,目前臨床主流的纈氨酸 - 瓜氨酸(Val-Cit)連接子即通過(guò)溶酶體酶切割實(shí)現(xiàn)定點(diǎn)釋放。
二、ADC 的 “降維打擊” 優(yōu)勢(shì):三大核心特性重塑治療邏輯
1. 突破靶向治療耐藥困境
當(dāng)靶向藥因抗原突變(如 EGFR T790M)或信號(hào)通路旁路激活失效時(shí),ADC 可通過(guò) “旁觀者效應(yīng)” 擴(kuò)大殺傷范圍 —— 釋放的毒素能穿透細(xì)胞膜,殺滅鄰近未表達(dá)靶抗原的癌細(xì)胞,尤其適合異質(zhì)性強(qiáng)的實(shí)體瘤(如三陰乳腺癌、非小細(xì)胞肺癌)。
2. 解鎖 “不可成藥” 靶點(diǎn)
針對(duì)傳統(tǒng)靶向藥難以作用的膜蛋白(如糖蛋白、黏附分子),ADC 展現(xiàn)獨(dú)特優(yōu)勢(shì):
- Claudin 18.2:全球首個(gè)獲批的 Claudin 18.2 ADC(Zolbetuximab)改寫(xiě)胃癌治療指南,對(duì) Claudin 18.2 高表達(dá)患者中位總生存期延長(zhǎng)至 13.2 個(gè)月;
- Trop-2:戈沙妥珠單抗(Sacituzumab govitecan)通過(guò)靶向 Trop-2,在三陰乳腺癌中客觀緩解率達(dá) 35%,成為首個(gè)獲批的 Trop-2 ADC。
ADC 的療效與 “藥物抗體比”(DAR)密切相關(guān),通過(guò)控制每個(gè)抗體連接 2-8 個(gè)毒素分子,在保證靶向性的同時(shí)避免抗體結(jié)構(gòu)破壞。以 HER2 陽(yáng)性乳腺癌為例,曲妥珠單抗 ADC(T-DXd)的 DAR 值達(dá) 8,較傳統(tǒng) T-DM1(DAR=3.5)療效提升 3 倍,且心臟毒性顯著降低。

三、全球市場(chǎng)爆發(fā):從 “小眾創(chuàng)新” 到 “百億賽道”
當(dāng)前全球已上市 16 款 ADC 藥物,2023 年市場(chǎng)規(guī)模達(dá) 138 億美元,預(yù)計(jì) 2030 年將突破 600 億美元,三大驅(qū)動(dòng)力加速行業(yè)變革:
1. 適應(yīng)癥快速擴(kuò)展
從血液瘤(如 CD19 ADC 治療 B 細(xì)胞淋巴瘤)到實(shí)體瘤(如 HER2 ADC 覆蓋胃癌、肺癌、乳腺癌),ADC 適應(yīng)癥已覆蓋 12 大癌種,僅 2023 年就有 5 款新藥獲批,包括首個(gè)雙特異性 ADC(REGN1500/RG7802)。
2. 技術(shù)平臺(tái)迭代升級(jí)
- 新型連接子:可裂解連接子(如 vc-MMAE)占比從 2015 年的 60% 降至 2023 年的 45%,不可裂解連接子(如硫醚連接子)因穩(wěn)定性?xún)?yōu)勢(shì)獲更多青睞;
- 雙抗 ADC:同時(shí)靶向兩個(gè)抗原(如 EGFR/c-Met),解決腫瘤抗原異質(zhì)性問(wèn)題,臨床前數(shù)據(jù)顯示其腫瘤富集效率提升 2 倍;
- 基因工程抗體:通過(guò) Fc 段改造降低 ADCC 效應(yīng)(如 IgG4 亞型),延長(zhǎng)藥物半衰期(如維迪西妥單抗半衰期達(dá) 14 天)。
榮昌生物(RC48)、恒瑞醫(yī)藥(SHR-A1811)、科倫博泰(SKB264)等本土企業(yè)引領(lǐng) ADC 研發(fā),全球在研 ADC 中 35% 來(lái)自中國(guó),適應(yīng)癥覆蓋 HER2、Claudin 18.2、c-Met 等熱門(mén)靶點(diǎn),部分產(chǎn)品(如 RC48)已獲 FDA 突破性療法認(rèn)定,開(kāi)啟 “中國(guó)創(chuàng)新藥出海” 新征程。
四、挑戰(zhàn)與未來(lái):從技術(shù)攻堅(jiān)到生態(tài)構(gòu)建
1. 三大核心技術(shù)瓶頸
- 脫靶毒性:抗原在正常組織低表達(dá)引發(fā)的副作用(如 T-DXd 的間質(zhì)性肺炎發(fā)生率達(dá) 13%),需通過(guò)雙抗靶向、時(shí)空可控釋放技術(shù)優(yōu)化;
- 耐藥機(jī)制:包括抗原下調(diào)(如 HER2 低表達(dá)腫瘤)、溶酶體功能異常、藥物外排泵激活,需聯(lián)合靶向藥(如 mTOR 抑制劑)或免疫治療(PD-1 單抗)破解;
- 生產(chǎn)工藝:ADC 的均一性控制(DAR 值分布)、穩(wěn)定性檢測(cè)(聚集態(tài)分析)對(duì) CMC 提出嚴(yán)苛要求,目前全球僅 12 家企業(yè)具備大規(guī)模生產(chǎn)能力。
- 多特異性 ADC:同時(shí)靶向腫瘤抗原與免疫檢查點(diǎn)(如 PD-L1/Her2 雙抗 ADC),實(shí)現(xiàn) “靶向殺傷 + 免疫激活” 雙重作用;
- 精準(zhǔn)患者篩選:建立基于抗原表達(dá)量(IHC 評(píng)分)、腫瘤微環(huán)境(基質(zhì)金屬蛋白酶水平)、藥代動(dòng)力學(xué)(ADC 清除率)的三維生物標(biāo)志物體系,如 Kadcyla 已將 HER2 IHC 3 + 作為核心入組標(biāo)準(zhǔn);
- 智能化設(shè)計(jì):利用 AI 預(yù)測(cè)抗體 - 抗原結(jié)合親和力(如 DeepMAB 平臺(tái))、毒素釋放動(dòng)力學(xué),將 ADC 研發(fā)周期從傳統(tǒng)的 5-7 年縮短至 3-4 年。
結(jié)語(yǔ):ADC 開(kāi)啟腫瘤治療 “精準(zhǔn)爆破” 時(shí)代
從 1913 年保羅・埃爾利希提出 “魔法子彈” 概念,到 2023 年 ADC 全球市場(chǎng)突破百億,人類(lèi)用百年時(shí)間將夢(mèng)想轉(zhuǎn)化為現(xiàn)實(shí)。這種融合抗體靶向性、毒素高效性、連接子智能性的創(chuàng)新藥物,不僅改寫(xiě)了 HER2 等經(jīng)典靶點(diǎn)的治療格局,更解鎖了眾多 “不可成藥” 靶點(diǎn)的治療潛力。
隨著雙抗 ADC、多毒素偶聯(lián)、AI 輔助設(shè)計(jì)等技術(shù)的突破,ADC 正從 “精準(zhǔn)制導(dǎo)導(dǎo)彈” 進(jìn)化為 “智能巡航導(dǎo)彈”—— 既能識(shí)別單個(gè)癌細(xì)胞的 “獨(dú)特標(biāo)識(shí)”,又能根據(jù)腫瘤微環(huán)境動(dòng)態(tài)調(diào)整攻擊策略。未來(lái),隨著精準(zhǔn)篩選體系的完善與聯(lián)合治療方案的成熟,ADC 有望與免疫治療、基因療法形成協(xié)同網(wǎng)絡(luò),共同構(gòu)建 “個(gè)性化精準(zhǔn)抗癌” 的全新生態(tài)。在這場(chǎng)對(duì)抗癌癥的持久戰(zhàn)中,ADC 不僅是一款藥物,更是開(kāi)啟腫瘤治療精準(zhǔn)化、智能化的鑰匙,引領(lǐng)人類(lèi)向 “治愈癌癥” 的終極目標(biāo)大步邁進(jìn)。
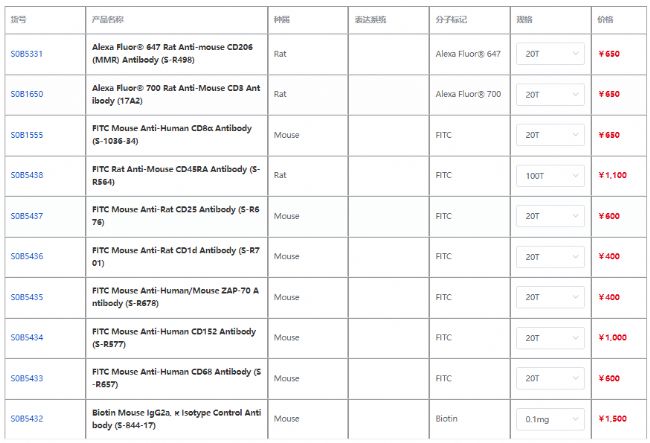
產(chǎn)品信息
杭州斯達(dá)特 (www.starter-bio.com)志在為全球生命科學(xué)行業(yè)提供優(yōu)質(zhì)的抗體、蛋白、試劑盒等產(chǎn)品及研發(fā)服務(wù)。依托多個(gè)開(kāi)發(fā)平臺(tái):重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開(kāi)發(fā)平臺(tái)(E.coli,CHO,HEK293,InsectCells),已正式通過(guò)歐盟98/79/EC認(rèn)證、ISO9001認(rèn)證、ISO13485。
- 腫瘤標(biāo)志物CA15-3在乳腺癌臨床管理中的應(yīng)用價(jià)值
- EGFR-TKI耐藥突變機(jī)制及治療現(xiàn)狀和應(yīng)對(duì)策略進(jìn)展
- 胃腸道間質(zhì)腫瘤診斷指標(biāo)DOG1/TMEM16A跨膜蛋白的調(diào)控機(jī)制
- 乳腺病理免疫組化從標(biāo)記物判讀到陷阱規(guī)避全指南
- 從樣品到WB的磷酸化蛋白檢測(cè)操作技巧
- 表觀遺傳之DNA甲基化的原理及檢測(cè)技術(shù)
- B淋巴細(xì)胞的發(fā)育、功能與免疫調(diào)控機(jī)制
- 生物素(Biotin)標(biāo)記技術(shù)的原理、方法與多領(lǐng)域應(yīng)用
- Agrisera直播:從抗體選擇到WB全流程優(yōu)化策略
- MCE中國(guó)抗體實(shí)驗(yàn)圖征稿啟示,秀美圖贏AirPods
- 斯達(dá)特生物將亮相2025年美國(guó)AACR展會(huì),誠(chéng)邀您蒞臨!
- MCE直播預(yù)告:銅死亡的機(jī)制探索與醫(yī)學(xué)應(yīng)用
- 2024第九屆疫苗中國(guó)領(lǐng)導(dǎo)者年會(huì)通知
- MCE推出超900種一抗和多種二抗產(chǎn)品,涵蓋熱門(mén)靶點(diǎn)
- 丹納赫將收購(gòu)Abcam以推動(dòng)生命科學(xué)領(lǐng)域研究創(chuàng)新進(jìn)程
- 睿捷生物新學(xué)期新福利,四重優(yōu)惠限時(shí)享
Copyright(C) 1998-2025 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com