YWHAG 缺失擾亂 EMT 相關網絡誘導氧化性細胞死亡并抑制癌癥轉移

發表期刊:ADVANCED SCIENCE
影響因子:14.3
發表年份:2023
作者單位:新加坡南洋理工大學
DOI:10.1002/advs.202301714
研究背景
癌癥轉移是晚期癌癥患者主要的死亡原因,其中上皮-間充質轉化(EMT)是癌細胞通過血液循環從原發部位遷移至遠端器官的重要過程。本研究聚焦于YWHAG(14-3-3γ蛋白編碼基因)在癌細胞EMT過程中調控作用,解析其作為腫瘤信號節點的機制及臨床意義。
轉移涉及上皮細胞向間質轉化(EMT),這一過程受復雜的基因網絡調控,故意破壞這些網絡可能會產生良好的結果。然而,人們對協調這些轉移相關網絡的機制知之甚少。為了填補這一空白,研究人員通過分析發生 EMT 的不同癌細胞類型的轉錄組,確定了在各種人類癌癥中具有廣泛參與性的樞紐基因。致癌信號適配蛋白酪氨酸3-單加氧酶/色氨酸5-單加氧酶活化蛋白γ(YWHAG)因其臨床相關性和影響而名列前茅。通過調查細胞激酶組和轉錄組數據,構建了 YWHAG 的調控組,揭示了癌癥 EMT 過程中的應激反應和代謝過程。研究表明,調控組中的YWHAG依賴性細胞保護機制嵌入了EMT相關網絡,通過增強EMT過程中的自噬作用保護癌細胞免受氧化災難。YWHAG 缺乏會導致活性氧(ROS)快速積累、EMT 延遲和細胞死亡。腫瘤異種移植顯示,轉移潛力和總生存時間與癌細胞株的 YWHAG 表達水平相關。與原發性腫瘤相比,轉移性腫瘤的 YWHAG 和自噬相關基因表達量更高。沉默 YWHAG 可減少原發腫瘤體積、防止轉移并延長小鼠的中位生存期。
研究成果
1. YWHAG 在EMT中的關鍵作用
- 通過轉錄組和蛋白相互作用數據,YWHAG 被鑒定為EMT調控網絡中的中心基因,廣泛參與多種癌癥類型的轉移過程。
- YWHAG 缺失顯著延遲了癌細胞EMT的發生,降低細胞間遷移距離,并誘導部分細胞發生間充質-上皮轉化(MET),從而抑制轉移能力。
2. YWHAG 的抗氧化保護機制
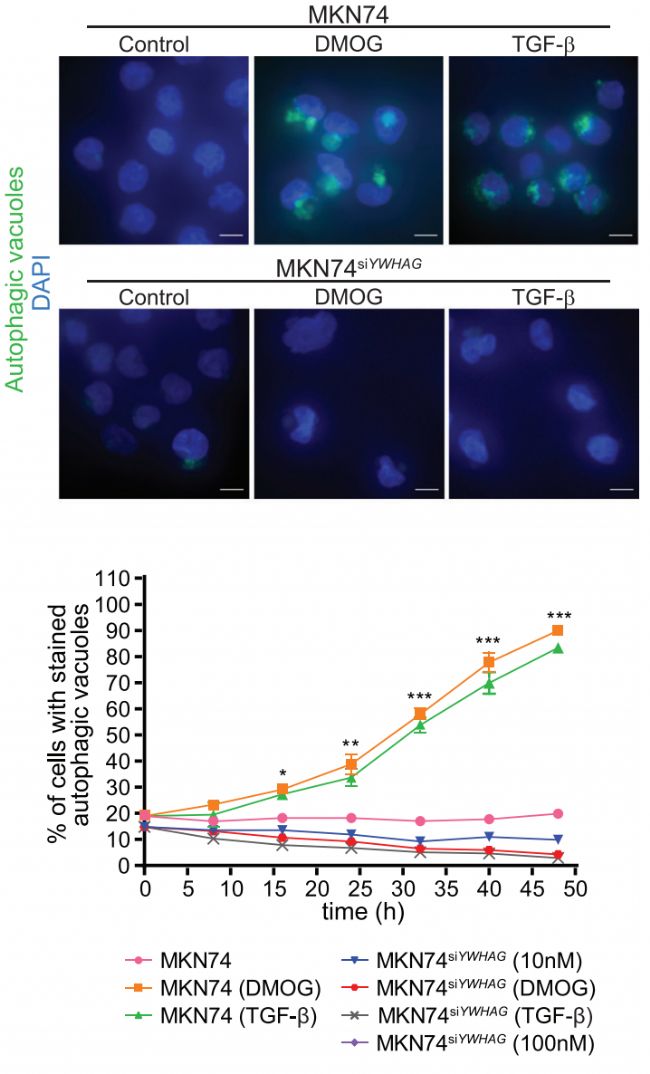
- EMT是高能耗過程,伴隨細胞內活性氧(ROS)水平顯著升高。YWHAG 通過增強細胞自噬緩解氧化應激,保護癌細胞免于氧化性細胞死亡。
- 在YWHAG 缺失的細胞中,ROS 水平急劇上升,導致細胞存活率顯著下降,凸顯其抗氧化機制的關鍵作用。
3. YWHAG 與腫瘤患者預后
- 分析多個癌癥數據庫(TCGA、GENT2等)顯示,在約70%的癌癥類型中,YWHAG 表達顯著上調,且高表達與患者較差的預后及較短的生存期相關。
- 動物模型實驗表明,YWHAG 缺失不僅抑制了原發腫瘤的生長,還減少了轉移灶的形成并延長小鼠的中位生存期。
4. YWHAG 調控網絡的潛在治療價值
- 整合YWHAG 依賴的蛋白激酶組、轉錄組及交互組學數據,研究構建了其調控網絡(regulome)。該網絡突出YWHAG 在細胞代謝和應激反應中的核心作用。
- 針對YWHAG 或其蛋白相互作用的靶向干預策略,如RNA干擾技術和小分子PPI抑制劑,可能為癌癥治療提供新路徑。
研究意義
本研究揭示了YWHAG 在EMT和腫瘤轉移中的關鍵調控作用,提出通過擾亂YWHAG 調控網絡可能成為抑制腫瘤轉移的新策略。這為開發基于非酶蛋白的治療手段提供了科學依據,也為改善晚期癌癥患者預后帶來潛在希望。
設備應用
激酶抑制劑陣列:用兩種激酶抑制劑(SYN- 2103;SYNkinase,澳大利亞維多利亞州;TargetMol,美國馬薩諸塞州)處理 MKN74 和 YWHAG 敲除的 MKN74(MKN74siYWHAG)細胞,這兩種激酶抑制劑由 188 種不同的小分子抑制劑組成,共針對 130 種獨特的蛋白激酶。使用JuLI™ Stage活細胞成像分析系統對處理過的細胞進行 48 小時成像。細胞群多元中心點之間的歐氏距離被視為遷移距離,在 48 小時內每隔 4 小時測量一次。遷移距離的時間變化以曲線下面積(AUC)表示,并在野生型 MKN74 和 MKN74siYWHAG 之間進行比較,以確定與 EMT 有關的蛋白激酶。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com