小鼠模型在眼科疾病研究中的應用與驗證數據解釋
近期,又一款眼科基因治療的新型藥物HG004獲得美國FDA授予的孤兒藥資格認定,用于治療由RPE65突變引起的遺傳性視網膜疾病。HG004注射液利用重組AAV載體遞送,在研發過程中,還使用到了Rpe65的基因敲除小鼠以模擬疾病患者的視網膜表型和功能。
出于眼睛的獨特結構,眼科疾病已成為基因治療的理想適應癥,隨著該療法日漸興起,臨床前對應的小鼠模型需求也日趨旺盛。在基因同源性方面,小鼠基因組與人類相似度近90%;在眼睛結構方面,小鼠的視錐細胞與視桿細胞數目比也與人類接近,因此,建立合適的小鼠模型已成為當前多數基因治療研究人員的不二選擇。
眼科疾病模型推薦
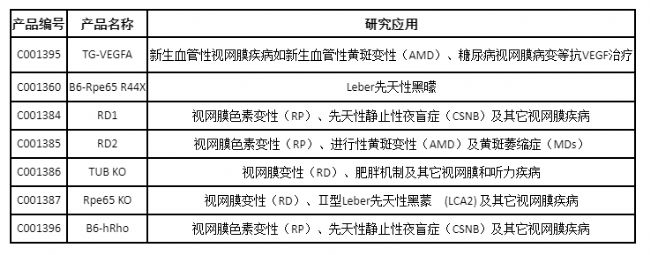
針對先天性黑蒙癥、進行性黃斑變性、視網膜色素變性、視網膜變性等眼科疾病,賽業生物開發了一系列基因編輯和人源化小鼠模型;針對研究人員的需求,也可定制或合作開發基因編輯小鼠模型,如基因敲除、基因敲入、點突變、人源化小鼠模型及大小鼠手術疾病模型,加速藥效學驗證實驗的開展。
驗證數據——以TG-VEGFA小鼠為例
這款自研的TG-VEGFA小鼠,是賽業生物建立的牛視桿細胞特異性啟動子驅動人源VEGFA基因CDS序列表達的模型,以獲得能在視網膜特異性過表達人源VEGFA基因的轉基因小鼠。
人源和鼠源VEGFA基因表達水平檢測
利用qPCR檢測小鼠體內人源VEGFA和鼠源VEGFA基因表達,結果顯示相比野生型小鼠,TG-VEGFA小鼠能高表達人源VEGFA,且鼠源VEGFA基因的表達量與野生型小鼠相當。表明該小鼠在過表達人源VEGFA的同時不會影響本底鼠源VEGFA的表達。
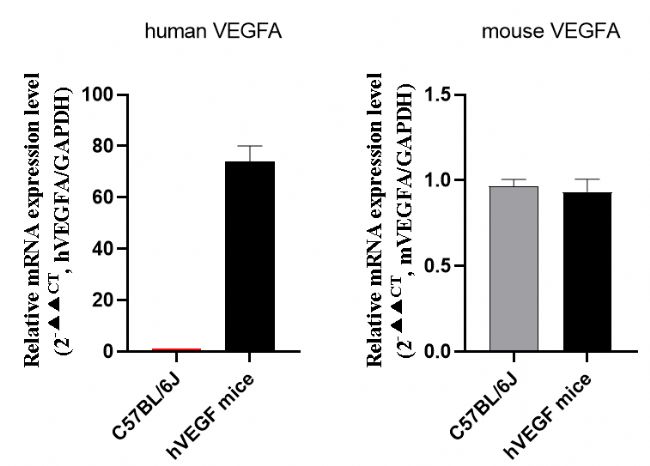
TG-VEGFA小鼠和C57BL/6J野生型小鼠中人源VEGFA和鼠源VEGFA基因表達的檢測
視網膜光學相干斷層掃描(OCT)檢測
通過視網膜光學相干斷層掃描(OCT)對小鼠的視網膜形態進行檢測,結果顯示與野生型相比,TG-VEGFA小鼠的脈絡膜區域的結構存在結構紊亂。
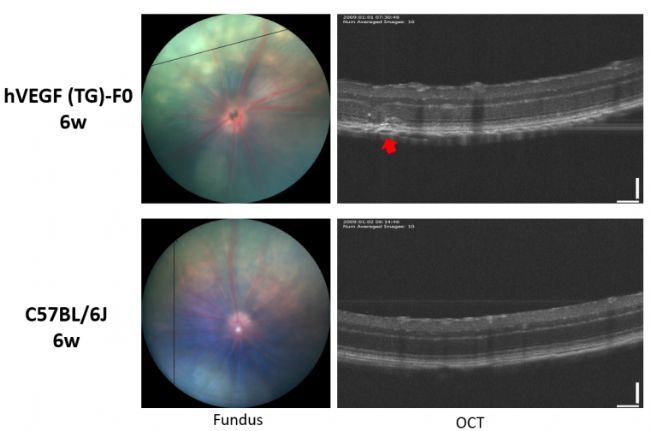
6周齡TG-VEGFA小鼠和C57BL/6J野生型小鼠的眼底和視網膜形態檢測
F0代小鼠眼底熒光血管造影(FFA)
通過FFA對小鼠的眼部血管進行造影觀察,結果顯示與野生型相比,TG-VEGFA F0代小鼠的眼底出現血管病變,表現為大面積熒光素鈉滲漏。
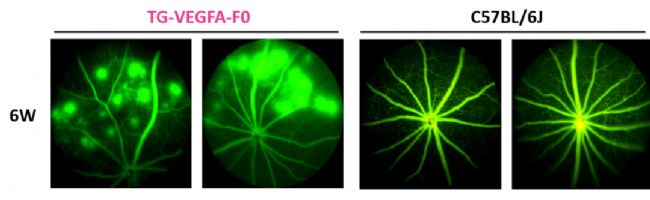
6周齡TG-VEGFA F0代小鼠和C57BL/6J野生型小鼠的眼底熒光血管造影(FFA)結果
F1代和F2代小鼠眼底熒光血管造影(FFA)
通過FFA對F1代和F2代的TG-VEGFA小鼠眼部血管進行造影觀察,結果顯示F1代和F2代小鼠均能復現F0代小鼠的表型,表現為大面積熒光素鈉滲漏的血管病變表型。
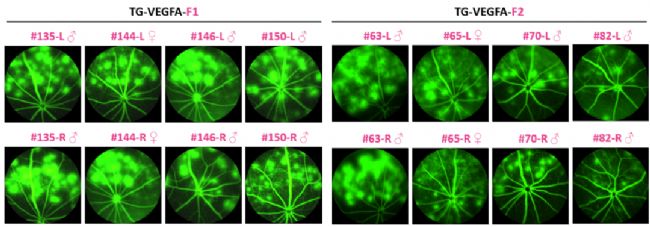
F1代和F2代TG-VEGFA小鼠眼底熒光血管造影(FFA)結果
視網膜電圖(ERG)檢查
視網膜電圖(ERG)的檢測結果顯示TG-VEGFA小鼠(hVEGFA)的視網膜電位與野生型小鼠(WT)暫無顯著差異。
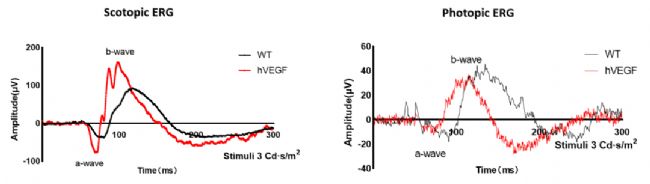
TG-VEGFA小鼠和野生型小鼠的視網膜電圖(ERG)檢測的結果
視網膜HE染色
通過HE染色對小鼠視網膜進行檢測,檢測結果顯示與野生型(C57BL/6J)相比,TG-VEGFA小鼠的視網膜區域存在血管增生的病理性表型。
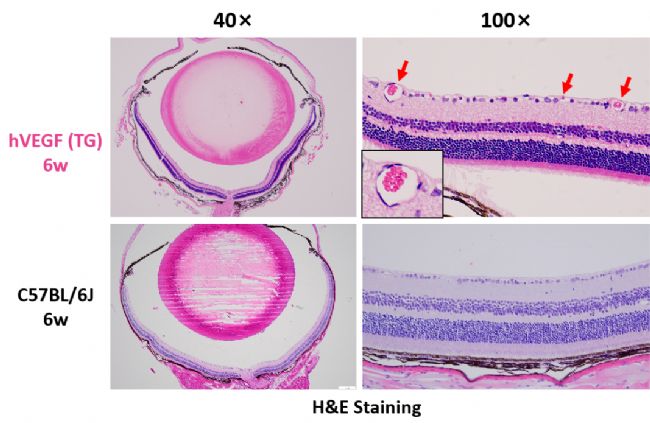
TG-VEGFA小鼠和野生型小鼠眼部HE染色結果
視網膜和脈絡膜isolectin GS-lB4免疫染色
通過lB4染色對小鼠視網膜和脈絡膜進行檢測,檢測結果顯示與野生型相比,TG-VEGFA小鼠的視網膜存在血管的異常增生,且結構紊亂,同時脈絡膜區域也觀察到有異常增生的情況。
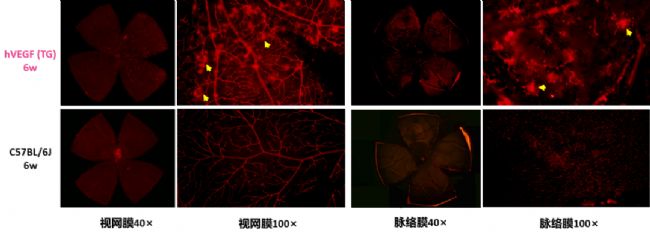
TG-VEGFA小鼠和野生型小鼠眼部視網膜和脈絡膜Isolectin GS-lB4免疫染色結果
阿柏西普(Aflibercept)藥效驗證
眼底熒光血管造影(FFA)的結果顯示,阿柏西普給藥前TG-VEGFA小鼠的眼底存在明顯的血管病變和大面積熒光素鈉滲漏。在阿柏西普給藥后,與PBS對照組相比,阿柏西普組中TG-VEGFA小鼠眼部血管病變顯著減輕,血管滲漏面積顯著減小。
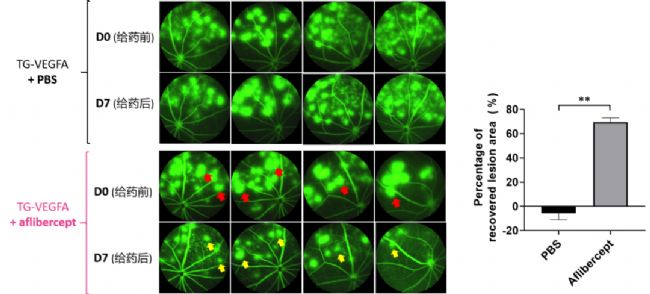
TG-VEGFA小鼠用于VEGF靶向藥物阿柏西普(Aflibercept)的藥效驗證