ЗеіэДНЛҺјҡҫъёРИҫЈәјtНв¶ю…^NIR©\II№вФцҸҠҙЯ»Ҝ»оРФј{ГЧГё

ҲD1 aЈәNIR-II№вн‘‘ӘөДCu2MoS4ј{ГЧІДБПҡўЛАјҡҫъөДКҫТвҲDЎЈ aЈ©ЦЖӮдCu2MoS4ј{ГЧІДБПЈЁCMS NPsЈ©Ј¬bЈ©NIR-II№вФцҸҠБЛCMS NPsөДлpЦШГёҙЯ»Ҝ»оРФЈ¬ҝЙФЪуwНвЗеіэДНЛҺөДҙуДc—UҫъәНҪрьSЙ«ЖПМСЗтҫъЈ¬cЈ©CMS NPsУГУЪЦОҜҹДНЛҺРФҪрьSЙ«ЖПМСЗтҫъөДуwғИёРИҫЎЈ
ДНЛҺјҡҫъХэФЪІ»”аіЙһйНюГ{ИЛоҗҪЎҝөөДТтЛШЦ®Т»ЎЈТтһйИұЙЩУРР§өДҝ№ЙъЛШЦОҜҹЈ¬И«ЗтГҝДкјsУР70ИfИЛҙОЛАУЪДНЛҺјҡҫъёРИҫЎЈТтҙЛЈ¬ЖИЗРРиТӘУРР§Мжҙъҝ№ЙъЛШөДІЯВФҒнҢҰҝ№ДНЛҺјҡҫъёРИҫЎЈ
»щУЪј{ГЧГёөДҙЯ»ҜЧчУГұ»ХJһйКЗҫЯУРқ“ФЪҝ№ҫъМШРФөДТ»·NЦОҜҹІЯВФЎЈј{ГЧГёДЬФЪДіР©—lјюПВЈ¬јӨ°lіц»оРФСхЈЁROSЈ©¶шҡўЛАјҡҫъЎЈ
Cu2MoS4ЈЁCMSЈ©КЗҫЯУРҸҠҙЯ»Ҝ»оРФөДИэФӘБтЧе»ҜОпЈ¬ФЪјtНв¶ю…^NIR-IIУРҸҠОьКХРФЈ¬ҫЯУРЧчһйјtНв¶ю…^NIR-II№вн‘‘Әј{ГЧҙЯ»Ҝ„©өДқ“БҰЎЈКЧПИЈ¬ЧчХЯЦЖӮдCMSІўҢўЖдЧціЙCMS NPsЈЁҲD1 aЈ©ЎЈ
КЧПИЈ¬ЧчХЯЦЖӮдіцәПЯmҙуРЎөДCMS NPsЈ¬НЁЯ^ңy¶ЁЈ¬ЖдЖҪҫщҙуРЎјsһй28 nmЈЁҲD1 aЈ©Ј¬әс¶Ијsһй12 nmЈЁҲD1 bЈ©ЎЈҙЛНвЈ¬ЧчХЯҢҰј{ГЧІДБПҳӢПс·ЦОцЈ¬°l¬FЖдёчФӘЛШФЪј{ГЧІДБПЦРҫщ„т·ЦІјЈЁҲD1 dЈ©ЎЈ

ҲD1ЈәCMS NPsөДұнХчЎЈaЈ©TEMҲDПсЈ¬bЈ©AFMҲDПсәНcЈ©CMS NPsөДHRTEMҲDПсЎЈdЈ©CMS NPsөДHAADF©\STEMҲDПсәНCuЈ¬MoәНSөДФӘЛШУіЙдҲDПсЈ¬ұИАэіЯһй20 nmЎЈeЈ©CMS NPsөДXRDҲDЧVЎЈCMS NPsЦРfЈ©Cu 2pЈ¬gЈ©Mo 3dәНhЈ©S 2pөДФӯЧУЬүөА·ЦОцҲDЎЈiЈ©CMS NPsөДFT-IR№вЧVЎЈ
лSәуЈ¬ЧчХЯңy¶ЁБЛCMS NPsөД№вҢWМШРФЎЈCMS NPsөДОьКХ№вЧVҸДЧПНв…^Т»ЦұСУЙмөҪNIR-II …^ЈЁҲD2 aЈ©ЎЈФЪУРјtНв¶ю…^NIR-IIјӨ№вХХЙдПВЈ¬CMS NPsөДЛ®ИЬТәҝЙФЪ10 min•rСёЛЩЙэңШөҪ39.3ЎжЈ¬ұн¬FБјәГөД№вҹбРФәН·Җ¶ЁРФЈЁҲD2 bЈ¬2 cЈ©ЎЈН¬•rЈ¬ФЪјtНв¶ю…^NIR-IIјӨ№вјӨ°lПВЈ¬CMS NPsҫЯУРБјәГөДоҗСх»ҜГёМШРФІўҝЙТФ®aЙъH2O2ЈЁҲD2 dЈ¬2 eЈ¬2 fЈ©ЎЈІ»ғHИзҙЛЈ¬јtНв¶ю…^NIR-IIјӨ№вЯҖДЬФцҸҠCMS NPsөДоҗЯ^Сх»ҜГёМШРФЈЁҲD2 gЈ©ЎЈ

ҲD2ЈәCMS NPsөД№вҢWМШРФЈ¬№вҹбМШРФәНоҗГёРФЩ|ЎЈaЈ©І»Н¬қв¶ИCMS NPsИЬТәөДUV-vis-NIRОьКХ№вЧVЈ¬bЈ©ФЪNIR-IIЈЁ1064 nmЈ¬1 W cm-2Ј©ПВөД№вҹбЗъҫҖЎЈcЈ©ФЪNIR-IIјӨ№вХХЙдЈЁ1064 nmЈ¬1 W cm-2Ј©ПВЈ¬CMS NPsЛ®ИЬТәЈЁ40 µg mL-1Ј©өДЦШҸНјУҹб/Ад…sЗъҫҖЎЈdЈ©ТФAAһйөЧОп•rЈ¬ңy¶ЁCMS NPsөДоҗСх»ҜГёМШРФЎЈeЈ©№ИлЧёКлДЕcІ»Н¬қв¶ИөДCMS NPs·хУэәуЈ¬ңy¶ЁЖд“pК§ВКЎЈfЈ©CMS NPsөДNIR-II№вФцҸҠоҗСх»ҜГёМШРФЎЈgЈ©ТФTMBһйөЧОп•rЈ¬ңy¶ЁCMS NPsөДоҗЯ^Сх»ҜГёМШРФЎЈhЈ©ңy¶ЁИэҪMИЬТәЦР•OHЙъіЙөДБҝЈЁҶОӘҡК№УГH2O2Ј¬H2O2 +CMS NPsЈ¬ТФTAЧчһйҹЙ№вЦёКҫ„©Ј©ЎЈiЈ©NIR-IIјӨ№вДЬФцҸҠCMS NPsөДоҗЯ^Сх»ҜГёМШРФЎЈ
ҪУПВҒнЧчХЯЧцБЛCMS NPsҢҰДНЛҺјҡҫъуwНвТЦЦЖөДҢҚтһЎЈФЪӣ]УРјtНв¶ю…^NIR-IIјӨ№в•rЈ¬лSЦшCMS NPsқв¶ИМбЙэЈ¬•юҢҰДНЛҺөДҙуДc—UҫъәНҪрьSЙ«ЖПМСЗтҫъЙъйL®aЙъТЦЦЖЧчУГЎЈН¬•rЈ¬ҪoУијtНв¶ю…^NIR-IIјӨ№вХХЙдәуЈ¬ғЙЦкјҡҫъЙъйLРФДЬ•юёьҙу·щ¶Иұ»ТЦЦЖЈЁҲD3 aЈ¬3 bЈ¬3 cЈ¬3 dЈ©ЎЈҪӣЯ^CMS NPs·хУэәуөДјҡҫъРО‘Bіц¬FІ»НкХыЈ¬ЖЖЛйөДёДЧғЈ¬јtНв¶ю…^NIR-IIјӨ№вХХЙд•юФцҙуДНЛҺҫъөДРО‘BёДЧғЈЁҲD3 eЈ¬3 fЈ©ЎЈЧчХЯЯҖ°l¬FЈ¬CMS NPsКЗНЁЯ^ФцјУуwПөЦРөДROSә¬БҝҒнТЦЦЖјҡҫъ»оРФЈ¬Н¬•rЯ@·NТЦЦЖМШРФЕcңШ¶ИөДЙэёЯкPВ“РФІўІ»ҙуЈЁҲD3 gЈ¬3 hЈ¬3 iЈ¬3 jЈ©ЎЈ
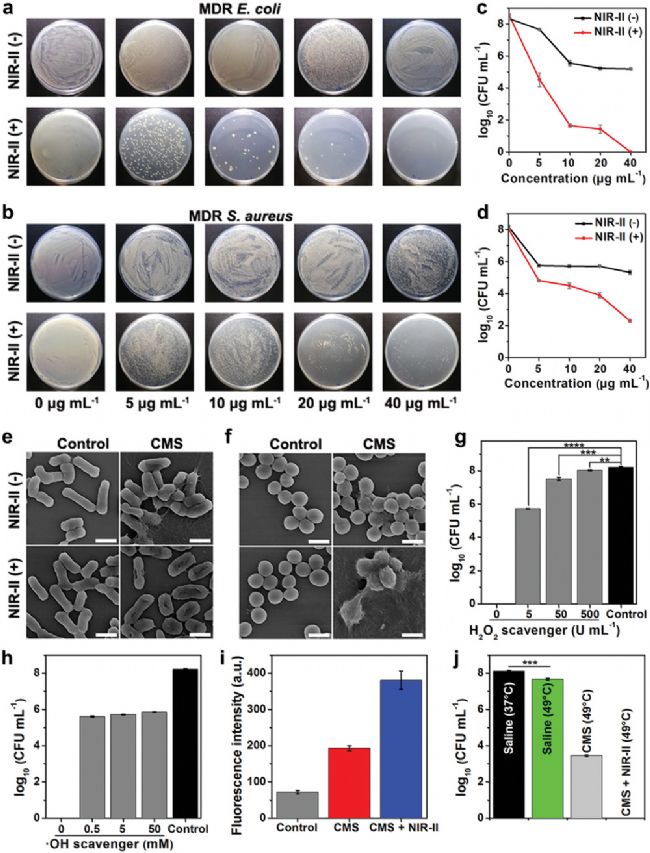
ҲD3ЈәCMS NPsөДуwНвҝ№ҫъ»оРФЎЈФЪУРҹoNIR-IIјӨ№вХХЙдЈЁ1064 nmЈ¬1 W cm-2Ј©әНІ»Н¬қв¶ИЈЁ0Ўў5Ўў10Ўў20әН40μg mL-1Ј©МҺАнөДaЈ©ДНЛҺРФҙуДc—UҫъәНbЈ©ДНЛҺРФҪрьSЙ«ЖПМСЗтҫъөДҫъВдХХЖ¬ЎЈCMS NPsЈЁ0Ўў5Ўў10Ўў20әН40 µg mL-1Ј©ЕccЈ©ДНЛҺРФҙуДc—UҫъәНdЈ©ҪрьSЙ«ЖПМСЗтҫъ№І·хУэәуөДҡўҫъР§ВКЎЈeЈ©ДНЛҺРФҙуДc—UҫъәНfЈ©ДНЛҺРФҪрьSЙ«ЖПМСЗтҫъФЪЙъАны}Л®ЈЁҢҰХХЈ©әНCMS NPs·ЦЙўТәЈЁ40 µg mL-1Ј©өДSEMҲDПсЈ¬ұИАэіЯЈ¬1 µmЎЈФЪNIR-IIјӨ№вХХЙдЈЁ1 W cm-2Ј©ПВЧчУГ10·ЦзҠЈ¬·Ц„eК№УГgЈ©H2O2Зеіэ„©ЈЁЯ^Сх»ҜҡдГёЈ©әНhЈ©•OHЗеіэ„©ЈЁ®җұыҙјЈ©Ј¬УӢЛгCMS NPsҢҰДНЛҺРФҙуДc—UҫъөДҡўҫъР§ВКЎЈiЈ©Фu№АCMS NPsМҺАнәуөДДНЛҺРФҙуДc—UҫъөДјҡ°ығИROSЛ®ЖҪЎЈjЈ©ёЯңШҢҰCMS NPsТЦЦЖДНЛҺРФҙуДc—Uҫъ»оРФөДУ°н‘ЎЈЈЁҫщЦө±SDЈ¬n = 3Ј¬** p <0.01Ј¬*** p <0.001әН**** p <0.0001Ј©ЎЈ
ҪУПВҒнЈ¬ЧчХЯМҪҫҝБЛCMS NPsқ“ФЪөДЦОҜҹЧчУГЎЈКЧПИЈ¬ЧчХЯҪЁБўБЛРЎКуҪрьSЙ«ЖПМСЗтҫъёРИҫДЈРНЈЁҲD4 aЈ©ЎЈФЪёРИҫІҝО»ЧўЙдCMS NPsЈЁ4 mg Kg-1Ј©әуЈ¬К№УГјtНв¶ю…^NIR-IIјӨ№вХХЙдЈЁ1064 nmЈ¬1 W cm-2Ј©5·ЦзҠЈ¬ЧўЙд…^ңШ¶ИЙэёЯ17ЎжЈ¬ЯhЯhі¬Я^ҢҰХХҪMЈЁҲD4 bЈ¬4 cЈ©ЎЈФЪЦОҜҹ16МмәуЈ¬ЦОҜҹҪM°Y оПыК§Ј¬ЕcҢҰХХҪMРОіЙп@ЦшІо®җЈЁҲD4 d-4 hЈ©ЎЈЯ@ұнГчCMS NPsҫЯУРБјәГөДЦОҜҹјҡҫъёРИҫөДДЬБҰЎЈ

ҲD 4ЈәCMS NPsөДуwғИҝ№ҫъСРҫҝЎЈaЈ©CMS NPsөДЦОҜҹЯ^іМЎЈҪӣCMS NPs әНы}Л®МҺАнөДРЎКуЖӨПВД“Д[…^өДbЈ©јtНвҹбҲDПсәНcЈ©ңШ¶ИЧғ»ҜЎЈdЈ©ФЪЦОҜҹәуөЪ0Ўў8әН16МмЈ¬РЎКуөДЖӨПВД“Д[ХХЖ¬ЎЈeЈ©ЦОҜҹәуРЎКуөДІЎЧғ…^УтҙуРЎЎЈЦОҜҹәуөЪ16МмІ»Н¬ҪMёРИҫ…^УтјҡҫъҫъВдfЈ©ХХЖ¬әНgЈ©ҫъБҝ·ЦОцЈЁҫщЦө±SDЈ¬n = 3Ј¬** p <0.01Ј©ЎЈhЈ©ФЪЦОҜҹәуөЪ16МмҪӣЯ^І»Н¬МҺАнәуөДёРИҫҪMҝ—HЈҰEИҫЙ«ҪY№ыЈ¬ұИАэіЯһй100 µmЎЈ
ҪYХ“ЈәЧчХЯй_°lБЛТ»·NҫЯУРлpЦШГёРФЎў№вҹбРФөДРВРНјtНв¶ю…^NIR-II№вн‘‘ӘөДҝ№ҫъј{ГЧГёCMS NPsЎЈФЪјtНв¶ю…^NIR-IIјӨ№вХХЙдПВЈ¬ЖдҫЯУРБјәГөД№вҹбРФДЬЈ¬Н¬•rҝЙТФ®aЙъҙуБҝөДROSЎЈФЪуwНвДЬүтҢҰДНЛҺРФҙуДc—UҫъәНҪрьSЙ«ЖПМСЗтҫъ®aЙъҡўӮыЎЈФЪЦОҜҹРЎКуДНЛҺРФҪрьSЙ«ЖПМСЗтҫъёРИҫ•rЈ¬CMS NPsДЬүтУРР§ңpЙЩСЧ°YЈ¬ЦОҜҹёРИҫЈ¬ҫЯУРЧчһйУРР§ҝ№ҫъ„©өДқ“БҰЎЈ
ОДХВҒнФҙЈәJingyang Shan, et al. Cu2MoS4 Nanozyme with NIR©\II Light Enhanced Catalytic Activity for Efficient Eradication of Multidrug©\Resistant Bacteria. Small, 2020.
⭐️ ⭐️ ⭐️
јtНв¶ю…^РЎ„УОп»оуwҹЙ№віЙПсПөҪy - MARS
NIR-II in vivo imaging system
ёЯм`Гф¶И - ІЙУГPrinceton InstrumentsЙоЦЖАдПаҷCЈ¬»оуwҙ©НёЙо¶ИёЯУЪ15mm
ёЯ·ЦұжВК - ¶ЁЦЖёЯ·Цұжҙу№вИҰјtНвзRо^Ј¬ҝХйg·ЦұжВКғһУЪ3um
ҹЙ№вүЫГь - ·ЦұжВКғһУЪ 5us
ёЯЛЩІЙјҜ - ЛЩ¶ИғһУЪ1000fps ЈЁҺ¬ГҝГлЈ©
¶аДЈ‘BПөҪy - ҝЙ”UХ№XЙдҫҖЭ—ХХЎўҹЙ№вүЫГьЎўТ»…^ҹЙ№віЙПсЎўФӯО»іЙПс№вЧVЈ¬CTөИ
п@ОўзR - јtНв¶ю…^ёЯ·Цұжп@ОўПөҪyЈ¬јжИЭіЙПсРН№вЧVғx
- °ЧЖӨ•шЈәPPLN‘ӘУГУЪҗәБУӯhҫіЦРөДІЁйLЮD“Q
- Prometheusі¬өНББёЯҫ«¶ИЙ«¶ИУӢФЪ HDRп@КҫУӢБҝоIУтөД‘ӘУГ
- АӯЙмХTҢ§өДғИЖӨјҡ°ыҶОҢУ“pӮыөДПакPСРҫҝ
- Т•ҫWДӨЙсҪӣ№қјҡ°ыҪӣIL-12-SCGF-ҰВҙ®”_ХTҢ§ёЙјҡ°ыСЬЙъөДЙсҪӣұЈЧoЧчУГ
- ҹбүәҷCЕcБт»ҜғxФЪФOУӢФӯАнЎў‘ӘУГҲцҫ°ј°јјРg…ў”өЙПөДІо®җ
- СӘ№ЬғИЖӨ-йgідЩ|ҙ®”_НЁЯ^ Notch РЕМ–тҢ„УИЛіЙ№Зјҡ°ыөДіЙ№З·Ц»Ҝ
- TRPV4 ТЦЦЖ„©әНҷCРөШ“әЙҢҰңpЭpСЧ°YөД…fН¬ЧчУГ
- I оҗ PI3Ks јӨ»оРЎБәҫWјҡ°ыЦРАӯЙмХTҢ§өДЧФКЙ
- ЧVиDСыДъ№Іё°өЪ¶юК®ҢГИ«ҮшјӨ№вјјРgЕc№влҠЧУҢW•юЧh
- қЙ…RЙъОп”yОўЦШБҰ3DЕарBПөҪyББПаПИЯMҜҹ·Ё„“РВ·е•ю
- өВҮшPicoQuant ГвЩMUniHarp”ө“юІЙјҜЬӣјюХэКҪЙПҫҖ
- АнјУВ“әП…ўјУЙҪөШ¶аИҰҢУЧғ»ҜЕcЩYФҙҝЙіЦАmАыУГҢWРg•ю
- ЙПәЈПӘНШББПаКЧҢГЙПәЈҸНлsуwПөі¬ҝм„УБҰҢW•юЧh
- Щҗ¶чҝЖғxСыДъ…ўјУ2025өЪҫЕҢГИ«ҮшҙЕРФІДБПЕcЖчјюҙу•ю
- ЙПәЈиӘиӨ”yф~оҗУ^ңyПөҪy…ўјУЯ^ф~ФOК©2025ҮшлHСРУ‘•ю
- ҸНј{ББПа2025ЦРҮш»ҜҢW•юлҠҙЯ»ҜЕcлҠәПіЙҮшлHСРУ‘•ю