過程分析技術PAT與模型預測控制MPC技術賦能IVCC的實時監控

IVCC:細胞培養工藝的核心量化指標
IVCC定義
IVCC(積分活細胞濃度) 定義為培養時間內活細胞濃度的累積積分值,反映生物反應器中活細胞總量的動態變化。其數學表達式為:
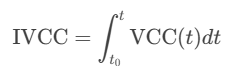
IVCC的工藝價值
積分活細胞濃度(IVCC)通過整合細胞培養周期內活性代謝能力的累積效應,成為生物制藥生產效率提升、工藝優化(補料策略)及質量控制的核心指標。

引用文獻[1]、[2]
在細胞培養過程中,傳統離線檢測活細胞濃度存在采樣頻率低、操作受人為干擾大等問題,導致 IVCC 計算偏差較大,實現實時監測活細胞濃度需要引入在線過程分析技術(PAT)。PAT:實時感知工具
過程分析技術(Process Analytical Technology, PAT)是由美國 FDA 倡導的框架,旨在通過實時測量生物工藝過程的關鍵質量和性能屬性,來設計、分析和控制生產過程。其核心目標是深刻理解并主動控制工藝過程,確保最終產品質量,實現“質量源于設計(QbD)”。
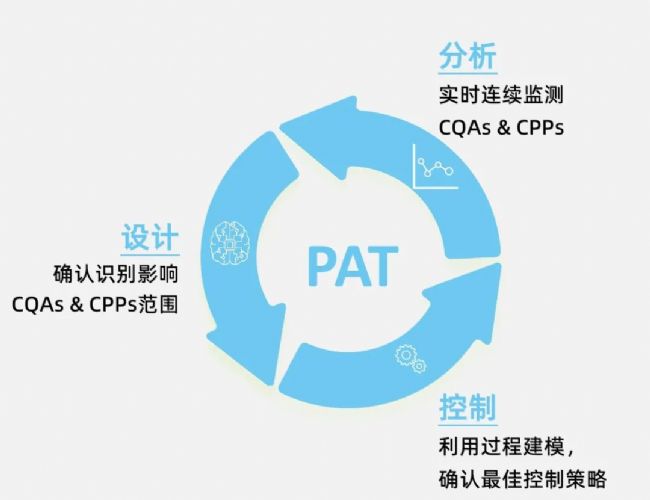
電容傳感器技術: 傳感器通過測量細胞懸浮液的介電特性變化,直接關聯活細胞密度。其優勢在于無需取樣、實時性強,適用于高密度細胞培養。[3]
拉曼光譜技術:拉曼光譜通過分析細胞代謝物(如葡萄糖、乳酸、氨基酸)的振動模式,間接反映細胞活性狀態。結合化學計量學模型,可建立代謝物濃度與IVCC的關聯,實現實時預測。[4]
光學傳感技術: 利用光波通過樣本時的相位變化構建圖像,反映細胞折射率分布,間接關聯細胞形態、厚度及干物質含量。
PAT的應用大幅減少對耗時的離線取樣的依賴,提供連續、高頻率的過程信息流,揭示傳統離線方法難以捕捉的過程動態和瞬態現象,高質量及高時效性的數據流為實施模型預測控制( MPC )技術等先進控制策略提供必需的輸入。
MPC:高級過程控制策略
MPC 是一種基于動態過程模型的高級過程控制策略。細胞培養工藝可通過模型預測控制器 (MPC) 來計算最優補料策略,從而在補料分批細胞培養過程中實現細胞生長和代謝物產量的最大化。[5]
模型構建
機理/數據驅動模型: 建立描述細胞生長、底物消耗、代謝產物生成及環境因素動態關系的數學模型。
IVCC預測模型: 將上述模型的核心輸出(如活細胞密度、生長速率)與IVCC計算關聯,構建能預測未來一段時間內IVCC軌跡的預測模型。
模型辨識與驗證: 利用歷史或實驗數據估計模型參數,并進行驗證,確保其能準確反映生物過程動態。
實施應用
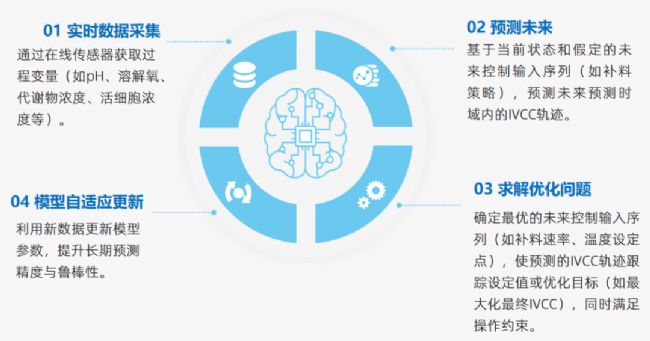
Akwa®PAT與特異性過程建模
Akwa®PAT是由浚真生命科學自主研發的在線分析和控制系統,包括Akwa®Cyte在線細胞傳感器、Akwa®Raman在線拉曼分析儀和Akwa®UV 在線純化和分離過程分析系統。助力生物制藥工藝過程中及早發現問題來改善工藝效率和生產率,通過密切監控關鍵質量屬性來確保產品質量及一致性,從而減少浪費、降本增效、實現高效工藝和技術轉移。
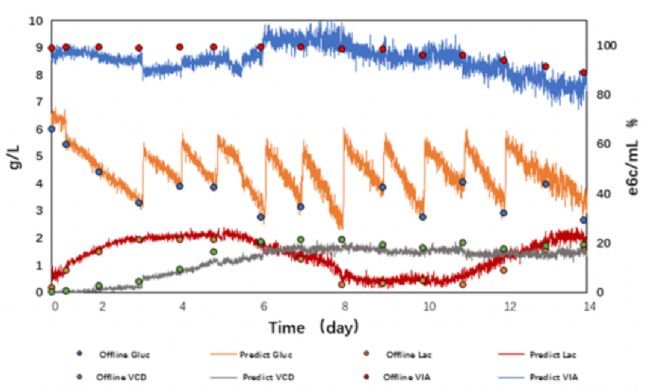

未來,隨著更先進的PAT工具、更強大的多模態建模與人工智能算法的發展,以及物聯網平臺的深度集成,將推動生物制藥工藝向高效、穩健、智能化方向持續發展。
參考文獻
[1]Ozturk, S. S., & Hu, W. S. (2006).Cell Culture Technology for Pharmaceutical and Cell-Based Therapies.CRC Press. Chapter 5.
[2]Pan, X.; Streefland, M.; Dalm, C.; Wijffels, R. H.; Martens, D. E. Selection of Chemically Defined Media for CHO Cell Fed-Batch Culture Processes. Cytotechnology 2017, 69 (1), 39–56.
[3]Weber, N. et al. (2018). "In-line monitoring of viable cell concentration using capacitance sensors in mammalian cell cultures." Journal of Biotechnology, 272–273, 42–49
[4]Zhang, L. et al. (2020). "Real-time monitoring of integral viable cell concentration in mammalian cell culture using Raman spectroscopy." Biotechnology and Bioengineering, 117(12), 3812–3823.
[5]Touraj Eslami, et al.(2024)Control strategy for biopharmaceutical production by model predictive control. Biotechnology Process, Volume 40, Issue2.
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com