ФЪҙуРНЙъОп·ҙ‘ӘЖчЦРЯMРРCHOјҡ°ыЕарB·ЕҙуөДСРҫҝ

CHOјҡ°ыЈЁЦРҮшӮ}КуВСіІјҡ°ыЈ©НЁіЈЧчһйЛЮЦчЙъ®aЦОҜҹУГөДЦШҪMө°°ЧЎЈлSЦшҝ№уwЛҺОпРиЗуөДҝмЛЩФцјУЈ¬CHOјҡ°ыФЪЙъ®aЦШҪMө°°ЧЦРЦрқuХј“юҪyЦОөШО»ЎЈCHOјҡ°ыөДіЙ№ҰТІөГТжУЪЖдФЪФзЖЪЦШҪMө°°ЧЦРөДіЙ№Ұұн¬FЈ¬УРТЧІЩЧчЎў°ІИ«·Җ¶ЁРФёЯЎўҝмЛЩ‘ТёЎЙъйLәНёЯө°°ЧұнЯ_өИғһ„ЭЎЈ

НЁіЈЈ¬ҢҰУЪПсРВ№ЪТЯГзЯ@оҗРиЗуБҝЭ^ҙуөДЛҺОпЈ¬•юК№УГ№ӨЧчуw·eһй100 – 2000 LЙхЦБёьҙуөДЙъОп·ҙ‘ӘЖчҒнқMЧгЙъ®aЎЈ¶шҢҰУЪЗ°ЖЪөДҢҚтһКТСР°lЎў№ӨЛҮй_°lәНФзЖЪЕRҙІФҮтһЈ¬НЁіЈЦ»•юК№УГТҺДЈЭ^РЎөД·ҙ‘ӘЖчЈЁ¶аһйОўРЎРНЕ_КҪ·ҙ‘ӘЖчЈ©ЎЈҢўЙъОп·ҙ‘ӘЖчҸДСР°lәНФзЖЪЕRҙІФҮтһЦРК№УГөДРЎуw·eЈЁ1-20 LЈ©”UҙуөҪЙМҳI»ҜТҺДЈЙъ®aЦРК№УГөДёьҙууw·eЈЁ100 – 2000 LЈ©ЙхЦБёьҙуЈ©Ј¬ІўЗТІ»п@ЦшёДЧғЕарBОпөДЙъАн о‘B»тјҡ°ыЙъОпҢWМШРФКЗкPжIЎЈ
ЯMРРІёИй„УОпјҡ°ы·ЕҙуЕарB•rЈ¬РиТӘҝј‘]ОпБП»мәП•rйgЈ¬СхЮDТЖПө”өәН¶юСх»ҜМјИҘіэЛЩВКөИкPжIТтЛШЎЈФЪЎ¶Scale-Up Analysis for a CHO Cell Culture Process in Large-Scale BioreactorsЎ·СРҫҝЦРЈ¬ҝЖҢWјТҢҰCHOјҡ°ыФЪҙуРНЙъОп·ҙ‘ӘЖчЈЁ5000LЈ©өД·ЕҙуЕарBЯMРРБЛ·ЦОцЎЈ
КЧПИЈ¬ФЪТ»Е_5000 LЙъОп·ҙ‘ӘЖчЦРЯMРРБЛ»мәПҢҚтһЈЁҹoјҡ°ыЈ©ЎЈПаН¬ЕдЦГПВЈ¬5000 L·ҙ‘ӘЖчЕcЕ_КҪ5 LәН20 L·ҙ‘ӘЖчПаұИЈ¬5000 LЙъОп·ҙ‘ӘЖчҫЯУРёьөНөДСхЮDТЖПө”өЎўёьйLөД»мәП•rйgәНёьөНөД¶юСх»ҜМјИҘіэВКЎЈ
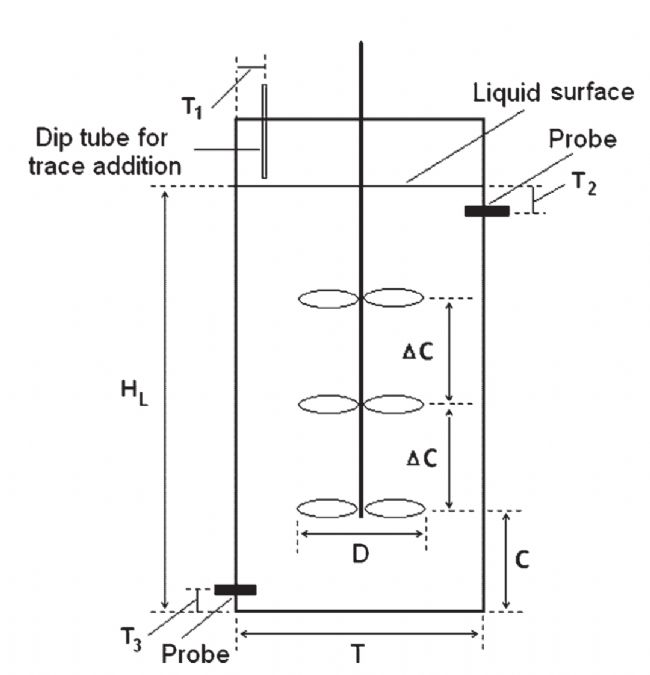


ЙъОп·ҙ‘ӘЖчЦР»мәП•rйgөДоAңyЈЁҫҖЈ©әНңyБҝЈЁ·ыМ–Ј©Цө
Н¬•rСхЮDТЖй“Цө·ЦОцұнГчЈ¬5000 L·ҙ‘ӘЖчөДЕдЦГЧоҙуЦ»ДЬЦ§іЦГҝәБЙэ7 x 10ЈЁ6Ј©ӮҖјҡ°ыөД»ојҡ°ыГЬ¶ИЎЈ
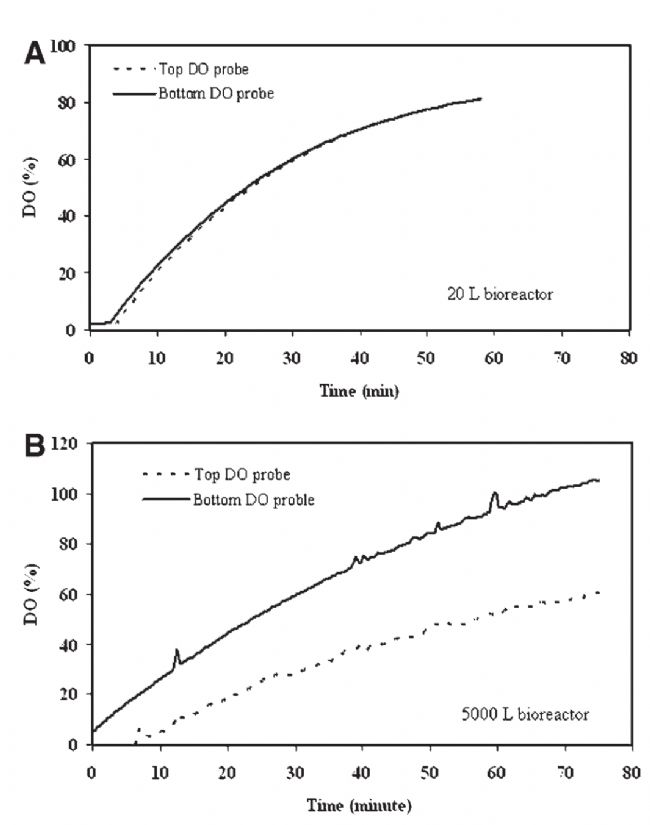 ЙъОп·ҙ‘ӘЖчИЬҪвСхұИЭ^
ЙъОп·ҙ‘ӘЖчИЬҪвСхұИЭ^
һйБЛҪвӣQЙПКцУ°н‘Ј¬ІЙУГҪӣтһ·ҪіМоAңy5000 LЙъОп·ҙ‘ӘЖчІ»Н¬…ў”өПВөД»мәП•rйgЎўСхЮDТЖПө”өәН¶юСх»ҜМјИҘіэВКЎЈҪY№ыұнГчЈ¬ФЪёДЙЖСхҡвЮDТЖПө”өәН¶юСх»ҜМјИҘіэВКЙПЈ¬ФцјУөЧІҝНЁҡвЛЩВКұИФцјУ№ҰВКЭ”ИлёьУРР§ЎЈ
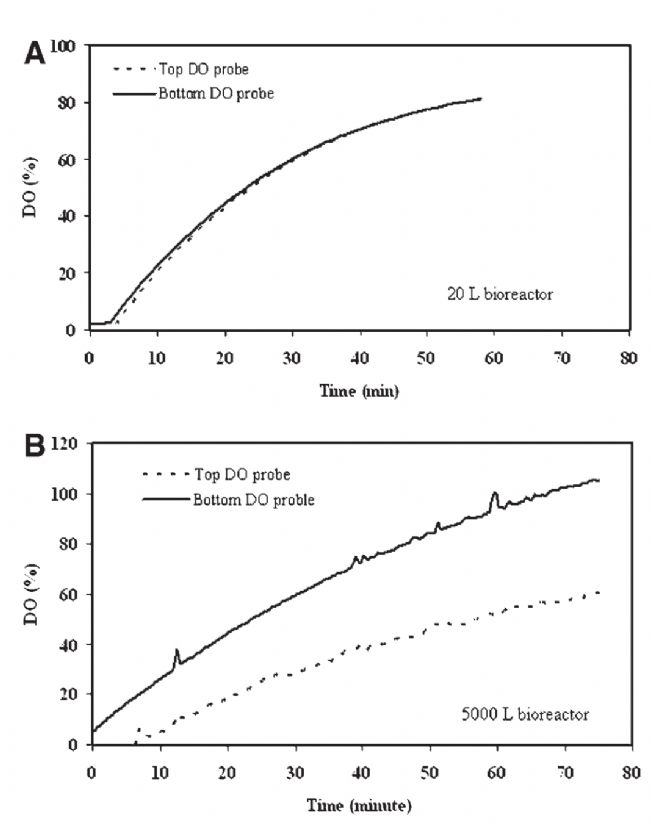 ¶юСх»ҜМјИҘіэВКЕcНЁҡвЛЩВКЎў№ҰВКЧғ»ҜкPПө
¶юСх»ҜМјИҘіэВКЕcНЁҡвЛЩВКЎў№ҰВКЧғ»ҜкPПөЈЁ№ҰВКЈә5.2 W/m³ - ІжЎў24 W/m³ - БвРОЎў100 W/m³ - ИэҪЗРОЈ©
СaБП·ЦЕъ°lҪНПВЙъОп·ҙ‘ӘЖчЦРТәуwуw·eөДФцјУЈ¬ҙуИЭ·eПВөДОпБП»мәПіЙһйТ»н—Мф‘рЎЈСРҫҝұнГчЈ¬5000 LЙъОп·ҙ‘ӘЖчЦРЕc»мәП•rйgЎў¶юСх»ҜМјИҘіэЛЩВКПакPөД№ӨіМ…ў”өҝЙДЬРиТӘғһ»ҜЈ¬ҸД¶шҪөөН№ӨЛҮ·Еҙу•rІ»Н¬пLлUіц¬FөДҝЙДЬРФЎЈ
…ўҝјОД«IЈә
1. Xing Z, Kenty BM, Li ZJ, Lee SS. Scale-up analysis for a CHO cell culture process in large-scale bioreactors. Biotechnol Bioeng. 2009 Jul 1;103(4):733-46. doi: 10.1002/bit.22287. PMID: 19280669.
 ……
……
ПВЖЪҫҙХҲА^АmкPЧў
В“ПөлҠФ’Јә021-57640001
E-mailЈәzhimengmeng@parallel-bioreactor.com
- јҡ°ыҜҹ·ЁөДғЙҙуәЛРД·ЦЦ§ј°ЖдФЪбtҢWФЩЙъоIУтөД‘ӘУГ
- ОўБчуwЙъОп·ҙ‘ӘЖч°Рјҡ°ыҝмЛЩҝШЦЖӮчёРЖҪЕ_№ӨЧчФӯАнј°‘ӘУГҪйҪB
- IKA HABITAT№вХХЙъОп·ҙ‘ӘЖчФЪОўФеЕарBЦРөД‘ӘУГ
- ОўЦШБҰЕарBПөҪyЦъБҰОўЙъОпЕcјҡ°ыСРҫҝ
- І»Н¬ҝЖСР‘ӘУГҲцҫ°ПВИзәОЯx“сОўЦШБҰРэЮDјҡ°ыЕарBПөҪy
- »щУЪ5LЕ_КҪЙъОп·ҙ‘ӘЖчөДОrЗаЛШёЯ®a·Еҙу№ӨЛҮСРҫҝ
- ЙъОп·ҙ‘ӘЖчЦъБҰ7.6ұ¶®aБҝМбЙэөДОrЗаЛШЙъ®a№ӨЛҮҝмЛЩғһ»Ҝ
- јҡ°ыЕарBОўЭdуwЈәІ»Н¬ІДБПөДғһИұьcј°‘ӘУГЦёДП
- °¬ШҗМ©Ңў”yЙъОп·ҙ‘ӘЖчөИ…ўјУCPHI&PMEC China 2025
- °¬ШҗМ©СыДъ…ўјУЙПәЈISPE 2025ҮшлHЦЖЛҺ№ӨіМҙу•ю
- °¬ШҗМ©”yЙъОп·ҙ‘ӘЖчөИББПаөЪ¶юК®ЛДҢГЙъОпЦЖЖ·ҙу•ю
- CytivaЛјНШ·І:“P·«УӢ„қ-ЧЯИл¶ҰҝөЙъОп»о„УҲAқMЕeРР
- DHSЈЁ¶Ұк»ФҙЈ©Х\СыДъ…ўјУөЪ24ҢГЦРҮшЙъОпЦЖЖ·ҙу•ю
- °¬ШҗМ©Х\Ңў”yЙъОп·ҙ‘ӘЖчөИ…ўјУЦРҮшЙъОпЦЖЖ·ҙу•ю
- °¬ШҗМ©”yЙъОп·ҙ‘ӘЖчөИББПаSBCәПіЙЙъОпҢW®aҳIІ©У[•ю
- °¬ШҗМ©СыДъ…ўјУSBC2025өЪИэҢГәПіЙЙъОпҢW®aҳIІ©У[•ю